El 20% de los españoles padece hígado graso o esteatohepatitis, y entre el 2 y el 3% ya ha desarrollado inflamación hepática o fibrosis, lo que puede acabar desembocando en casos graves de cirrosis o cáncer hepático.
Los expertos reunidos en el XXXIX Congreso Anual de la Asociación Española para el estudio del Hígado (AEEH) han presentado un nuevo método diagnóstico para detectar esteatohepatitis no alcohólica (EHNA o NASH por sus siglas en inglés) sin necesidad de realizar una biopsia. La esteatohepatitis es una enfermedad del hígado que se produce por la inflamación y daño de este órgano, como consecuencia de una acumulación excesiva de grasa en forma de triglicéridos, en lo que se conoce como enfermedad del hígado graso (HGNA o NAFLD).
Considerada como una de las epidemias clínicas del siglo XXI debido al consumo generalizado de una dieta excesivamente calórica, el hígado graso se produce por «la acumulación de ácidos grasos y triglicéridos en las células hepáticas. Su origen es desconocido aunque suele ir asociado a la obesidad, la diabetes y la hiperlipidemia, y cuando esta infiltración grasa se complica, el hígado se inflama y aparece la esteatohepatitis, una enfermedad que debe ser tratada precozmente porque puede desembocar en cirrosis o cáncer», explica el Dr. Manuel Romero, miembro de la AEEH y catedrático de medicina de la Universidad de Sevilla.
La esteatohepatitis es una enfermedad completamente asintomática, que genera una pequeña alteración de la bioquímica hepática junto con alteraciones metabólicas (síndrome metabólico) como la hipertensión, obesidad, dislipemia, diabetes, etc.
La detección de hígado graso ocurre muchas veces en un chequeo rutinario y es confirmado mediante una simple analítica de sangre o una ecografía. Ahora bien, el diagnóstico de la esteatohepatitis es un poco más complejo ya que requiere de la realización de una biopsia, por lo que es mucho menos accesible e incomodo para el paciente. «Justamente por este motivo se ha desarrollado un nuevo método diagnóstico capaz de detectar si el paciente padece inflamación hepática a través de una resonancia magnética y, mediante un posterior análisis en el ordenador, nos mostrará su diagnóstico con una seguridad claramente superior a los métodos de los que disponemos a día de hoy», destaca el Dr. Manuel Romero.
Actualmente, en torno al 20 por ciento de los españoles padecen hígado graso, cifra que está aumentando potencialmente entre los jóvenes. Entre un 10 y 15 por ciento de los pacientes con hígado graso desarrollan esteatohepatitis, lo que representa un 2-3% de la población total española o lo que es lo mismo, más de un millón de personas.
Esta inflamación hepática, caracterizada por la acumulación de grasa, es producida principalmente por dos causas diferenciadas: por el consumo de alcohol en exceso (esteatohepatitis alcohólica) y por tener un perfil de obesidad o diabetes (esteatohepatitis no alcohólica). Aún así, en los últimos estudios realizados, se ha detectado que entre un 30% – 40% de los pacientes que presentan una esteatohepatitis no alcohólica es debido a causas genéticas. «Se ha comprobado que la presencia de una mutación en el gen PNPLA3 puede conllevar a que la persona sea más propensa a acumular grasa en el hígado y, por tanto, a desarrollar esta enfermedad sin necesidad de tener unos perfiles clínicos desfavorables. Se calcula que solo el 3%-5% de la población española tiene este gen mutado y que más de un tercio de ellos tendrán tendencia a desarrollar enfermedad hepática», puntualiza el Dr. Romero.
Las dos complicaciones más graves que derivan directamente de esta enfermedad serían, por un lado, la progresión natural de la enfermedad hepática, es decir, un primer proceso a la cirrosis que podría llegar a producir cáncer de hígado, y, por otro, el incremento del riesgo cardiovascular, ya que se ha visto que las personas que poseen el hígado inflamado tienen mayor riesgo cardiovascular que las personas con hígado sano.
A pesar de ello, la esteatohepatitis es una enfermedad que se puede revertir mediante la práctica regular de ejercicio físico y una dieta saludable, junto con el control de las principales enfermedades que se asocian a la esteatohepatitis, como es la obesidad y la diabetes. Aun así, el Dr. Manuel Romero añade que, «el problema es que resulta tremendamente difícil convencer al paciente para que haga deporte, con lo que nos vemos obligados a desarrollar nuevos tratamientos que permitan lograr el control de la enfermedad». En este sentido, también se presentará en el congreso un estudio que muestra el impacto positivo del ejercicio físico y la dieta durante un año en esta enfermedad. Además, en el marco del congreso, se discutirán las posibilidades terapéuticas de fármacos prometedores como el ácido obeticólico, la quercetina o el GFT-505″, añade el hepatólogo.
En el marco de la AEEH se ha conformado el Grupo Nacional para el Estudio de la Esteatohepatitis, un equipo formado por dieciocho grupos de investigación, quince hospitales y tres centros de investigación básica, que tiene el objetivo de elaborar el primer registro sobre esta enfermedad y potenciar la investigación traslacional y de colaboración.
Los hepatólogos españoles reclaman una estrategia nacional en hepatología
El Congreso ha albegado la presentación del Libro Blanco de la Hepatología en España, una iniciativa liderada por la AEEH, con la colaboración de Porib y Gilead, que pretende poner de manifiesto el rol de la hepatología en nuestro país, dando a conocer datos sobre los recursos asistenciales, humanos, diagnósticos y terapéuticos, que están disponibles actualmente para el manejo de estos pacientes.
Gracias a este trabajo, en el que han participado un total de 161 hospitales españoles de referencia, sabemos, por primera vez, que nuestro país dispone de un total de 590 médicos destinados al manejo de los pacientes hepáticos (ratio de 1,28 por cada 100.000 habitantes), y que, además, el 56% de estos especialistas se localizan en los hospitales de más de 500 camas y que poseen una edad media de 47 años.
El documento también revela que la mortalidad asociada a las enfermedades hepáticas (8%) duplica la tasa de mortalidad por cualquier otra causa dentro de los servicios hospitalarios de gastroenterología y medicina interna (3%) y la tasa de mortalidad de los hospitales consultados (4%). Además, las enfermedades hepáticas son responsables del 2% del total de ingresos que se produjeron en nuestro país en el año 2011 (3.640.064), y es la segunda enfermedad que ha experimentado un mayor crecimiento en el número de ingresos en los últimos cinco años.
Otro dato analizado en la investigación realizada por la AEEH, ha sido saber cuales son las patologías hepáticas más frecuentes de las consultas externas, es decir, aquellas revisiones que realiza el especialista a aquellos pacientes que ya no están hospitalizados. Así, se ha visto que el 80% de las consultas se debieron a hepatitis virales (36%), trasplante hepático (27%) y cirrosis (16).
En este sentido el Dr. Calleja señala que «estos datos nos hacen preveer que la carga asistencial asociada a las patologías hepáticas irá en aumento durante los próximos años, con lo que es necesario que las autoridades sanitarias se comprometen a diseñar una estrategia nacional en hepatología, que pueda garantizar una calidad asistencial a todos los pacientes».
Fuente: Jano Online.
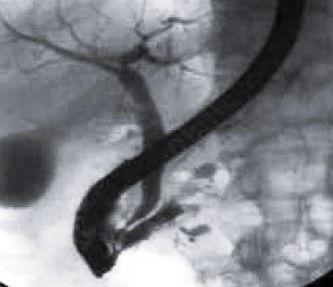 En este artículo se revisan las generalidades anatómicas, técnicas del procedimiento, indicaciones, contraindicaciones y complicaciones de la CPRE.
En este artículo se revisan las generalidades anatómicas, técnicas del procedimiento, indicaciones, contraindicaciones y complicaciones de la CPRE. La editorial Elsevier (Ciencia y Tecnología), ha concedido otorgar un período de prueba, para toda la red Infomed, a su plataforma
La editorial Elsevier (Ciencia y Tecnología), ha concedido otorgar un período de prueba, para toda la red Infomed, a su plataforma 










Los lectores comentan