El estudio explica cómo una proteína de la hepatitis C determina la falta de respuesta del sistema inmunológico hacia el virus, lo que podría explicar que en el 80% de los casos la infección se cronifique.
El grupo de investigación de la Universidad de Cádiz (UCA) que dirige el profesor Francisco García Cózar ha publicado un artículo en la revista Plos One en el que describe los mecanismos implicados en la cronificación de la infección por el virus de la hepatitis C. «Al conocerse que el virus de la hepatitis C utiliza una de sus proteínas para que el sistema inmune no responda –señala el estudio–, se podrá bloquear dicho proceso y lograr que el sistema inmunológico destruya el virus para evitar la hepatitis crónica».
Según indica la Fundación Descubre, los científicos de la UCA describen en células primarias cómo una proteína del virus de la hepatitis C (HCV) determina la falta de respuesta del sistema inmunológico hacia el virus. Esto «puede explicar que en el 80 por ciento de los casos la infección se cronifique, pudiendo derivar en cirrosis y hepatocarcinoma».
La investigación se enmarca en el área de la tolerancia inmunológica, en la que el equipo de científicos «cuenta con una larga trayectoria investigadora». Cuando un linfocito encuentra el antígeno que encaja con su receptor, empieza a dividirse generando un clon para destruir el antígeno. Algunos antígenos «pertenecen al propio organismo y deben ser preservados, pues de lo contrario se desarrollan enfermedades autoinmunes». Esto es la tolerancia inmunológica, «que puede definirse como la ausencia específica de respuesta del sistema inmune frente a autoantígenos».
«En general, siempre hemos investigado la tolerancia intentando inducirla para evitar enfermedades autoinmunes o el rechazo a trasplantes, y ahora pensamos que también puede ser aprovechada por los patógenos para que se les tolere a ellos, dando lugar a infecciones crónicas», ha indicado García Cózar.
Una proteína que permite activar el NFAT
En ensayos anteriores el grupo de la UCA había identificado que la molécula NFAT «estaba implicada, cuando se activa en solitario, en los mecanismos que permiten tolerar los autoantígenos». Por otra parte, un equipo de científicos del Instituto Karolinska de Estocolmo (Suecia) «comunicó que la proteína de la cápside del virus de la Hepatitis C era capaz de activar NFAT».
La cápisde es una estructura proteica, una cubierta protectora, en cuyo interior se encuentra el material genético del virus. «En ese momento nos dimos cuenta de que esa proteína del virus HCV estaba implicada en la no respuesta del sistema inmune y planteamos la hipótesis de que la proteína activa la molécula NFAT como un mecanismo de evasión del virus, para inducir la tolerancia inmunológica», señala García Cózar.
«De un modo más concreto, los científicos gaditanos describieron en 2007 que la cápside del virus de la Hepatitis C, llamada core, induce un mecanismo de tolerancia inmunológica denominado anergia», recalca la nota de la Fundación Descubre. Se trata de un proceso que consiste en «parar funcionalmente a los linfocitos, lo cual podría explicar por qué los linfocitos de muchos pacientes infectados por HCV no pueden eliminar el virus».
Más adelante, en 2011, demostraron que las células que tienen dentro la proteína vírica, «no sólo no responden, sino que son capaz de bloquear la respuesta de otros linfocitos». Estas demostraciones se hicieron en células tumorales, «con las que resulta más fácil trabajar».
En cambio, una de las novedades del ensayo descrito en el artículo publicado en Plos One es que «por primera vez se han realizado estos experimentos con células de la sangre, células primarias no tumorales, demostrando no sólo que no responden y que pueden bloquear otros linfocitos, sino que además una única proteína viral, la cápside del virus de la hepatitis C, era capaz de provocar un fenotipo de células agotadas, que son típicas de las infecciones crónicas y de los tumores».
De este modo «se explica por qué el sistema inmune no es capaz de eliminar el virus desarrollando una infección crónica». Para introducir la proteína del virus de la Hepatitis C en células de la sangre han utilizado como vector un lentivirus derivado del virus del Sida (VIH). Los lentivirus son un tipo de retrovirus que deben su nombre al hecho de que tardan mucho tiempo en desarrollar la enfermedad.
Linfocitos humanos de biobanco
Los retrovirus en general, al entrar en la célula, generan un ADN copia e integran esa información en el genoma de la célula infectada. Los investigadores de la UCA «han introducido la información correspondiente a la proteína de la cápside de la Hepatitis C sustituyendo el genoma del VIH, por lo que las células infectadas por este virus recombinante expresarán esta proteína en vez de proteínas del VIH».
García Cozar explica que «sustituimos el genoma del lentivirus por el gen que codifica para la proteína del virus de la Hepatitis C, seguida de una proteína que emite fluorescencia verde y, por otro lado, obtuvimos linfocitos humanos de biobanco, que infectamos con los lentivirus generados».
«Las células que de este modo expresan la proteína de la cápside de HCV y que podemos seguir por emitir fluorescencia verde, mandaban a su membrana una serie de moléculas inhibidoras y eran capaces de suprimir a otra célula que tenían al lado, que no podían dividirse a pesar de que su receptor para el antígeno estaba siendo estimulado», concluye el responsable del estudio.
Fuente: Jano Online.
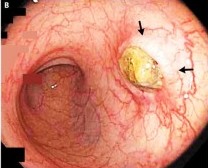 Review article: the pathogenesis and management of acute colonic diverticulitis.
Review article: the pathogenesis and management of acute colonic diverticulitis.









Los lectores comentan