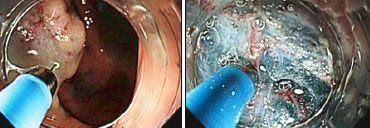
 Disección submucosa endoscópica: indicaciones, resultados y posibilidades de desarrollo en España.
Disección submucosa endoscópica: indicaciones, resultados y posibilidades de desarrollo en España.
Autores: JL Vila y cols. Fuente: Rev. esp. enferm. 2013; 105(9).
Desde la perspectiva de la práctica de esta técnica en España y otros países europeos, los autores de este artículo hacen una revisión de las indicaciones y resultados de la disección submucosa endoscópica (DSE). SE trata de una técnica que permite la resección curativa mediante endoscopia de lesiones malignas o premalignas superficiales digestivas en una sola pieza. Nacida hace algo más de 10 años en Japón, no ha experimentado una gran difusión en países occidentales por diferentes motivos, los que se comentan en el trabajo.
. En: NotiGastro. ![]()
Los últimos estudios en ratones sugieren que la translocación de algunas bacterias grampositivas puede influir en la respuesta a la quimioterapia.
La composición del microbioma podría tener un papel importante no sólo en el desarrollo de algunas enfermedades, sino también en la respuesta del organismo a algunos tratamientos, como podría ser el caso de la quimioterapia, según ha quedado de manifiesto durante un workshop sobre Genómica Traslacional en Biomedicina, organizado por Sergi Castellví-Bel, Meritxell Gironella, Cristina Fillat, Sílvia Beà y Lluís Hernández, del Instituto de Investigaciones Biomédicas August Pi i Sunyer (Idibaps), que se celebra estos días en Barcelona.
Los estudios más recientes, realizados en modelos animales de ratón, han evidenciado que la translocación de unas determinadas bacterias tipo grampositivas hacia los ganglios linfáticos secundarios se asocia a un incremento de la respuesta inmune de las células Th17, lo que mejora la respuesta a la quimioterapia, según ha explicado a Diario Médico Patricia Lepage, del Grupo de Funcionalidad del Ecosistema Intestinal del Instituto Francés de Investigación sobre Agricultura(INRA, por sus siglas en francés), en Jouy-en-Josas (Francia).
«Esto se debe al reclutamiento de unas células específicas que reducen el tamaño del tumor», ha comentado la investigadora, que ha ofrecido la ponencia titulada Secuenciación de nueva generación del microbioma intestinal, durante la jornada.
La quimioterapia destruye la barrera epitelial, lo que favorece la movilidad de las bacterias de la microbiota hacía los ganglios linfáticos. Esto abre la puerta a nuevas investigaciones sobre el posible papel de las bacterias como herramienta para mejorar los resultados de otros tratamientos.
Estudios previos habían sugerido que modelos animales de ratón con cáncer de mama que recibían antibióticos -que se sabe que alteran la composición de la microbiota intestinal- mostraban una peor respuesta terapéutica a la quimioterapia.
Por otra parte, Lepage ha comentado que la metagenómica abre la puerta a la investigación con muchas bacterias cuya función se desconoce hasta ahora porque no se pueden cultivar.
. En: NotiGastro. ![]()
Un nuevo estudio publicado en Cell Host & Microbe identifica una bacteria específica que aumenta o disminuye de forma anómala al desarrollarse la enfermedad.
Un estudio multiinstitucional revela que la microflora intestinal interpreta un papel importante en la respuesta inmune anómala de la enfermedad de Crohn. Además, los investigadores han identificado una bacteria específica que aumenta o disminuye de forma irregular cuando se desarrolla la enfermedad. Estos resultados, publicados en Cell Host & Microbe, sugieren cuáles de los metabolitos de la microbiota pueden ser el objetivo para tratar a los pacientes.
28 centros gastroenterológicos de Norteamérica han participado en el estudio. Los investigadores recogieron biopsias de 447 individuos con la enfermedad recién iniciada y 221 muestras de múltiples localizaciones a lo largo del tracto gastrointestinal de personas no afectadas. También validaron sus métodos en otros individuos, por lo que recogieron un total de 1.742 muestras tanto de pacientes pediátricos como adultos con la enfermedad recién iniciada o ya establecida.
El equipo de investigadores descubrió que el equilibro microbiótico se interrumpía en los pacientes con la enfermedad de Crohn, donde faltaban los microbios beneficiosos y prosperaban los patológicos. «Nuestro estudio ha identificado organismos específicos que aumentan o disminuyen de forma anómala en la enfermedad, lo que nos proporciona un punto de partida para desarrollar terapias microbióticas», explica Ramnik Xavier, autor del trabajo.
Cuando los científicos analizaron los efectos de los antibióticos, que se usan a veces para tratar los síntomas de la enfermedad crónica antes de diagnosticarla, descubrieron que este uso en los niños con la enfermedad podría ser contraproducente porque causa una pérdida de los microbios buenos y aumenta los patológicos.
Además, estudiaron distintos métodos para medir la cantidad de microbios buenos en los pacientes y descubrieron que las comunidades bacterianas en las biopsias extraídas del tejido rectal servían como un buen indicador de la enfermedad, independientemente de en qué parte del tacto gastrointestinal se produjera la inflamación. «Este hallazgo es particularmente esperanzador, ya que crea la oportunidad de utilizar un acercamiento mínimamente invasivo para recoger muestras de los pacientes para la detección precoz de la enfermedad», concluye Dirk Gerves, autor principal.
Fuente: Diario Médico 12/03/2014
. En: NotiGastro. ![]()
El punto de estudio es que la microbiota puede iniciar el proceso inflamatorio asociado a la obesidad.
Los estudios iniciales de la relación entre obesidad y la microbiota intestinal y su genoma, microbioma, indicaron que la microbiota podía desempeñar una función importante en el metabolismo energético. Con posterioridad, se ha avanzado en estas investigaciones y se ha descubierto que además la microbiota puede iniciar el proceso inflamatorio que está asociado a la obesidad. Según ha explicado a DM Yolanda Sanz, investigadora del Consejo Superior de Investigaciones Científicas en el Instituto de Agroquímica y Tecnología de Alimentos de Valencia (IATA-CSIC), esta conexión tiene aún mayor relevancia, ya que «la inflamación asociada a la obesidad es lo que causa las patologías crónicas que constituyen un serio problema de salud pública como el síndrome metabólico, diabetes tipo 2, ateroesclerosis o enfermedades cardiovasculares», que están contribuyendo a aumentar las tasas de morbilidad y reduciendo la esperanza de vida en nuestra sociedad.
Para Sanz, ponente en la jornada Microbioma y Obesidad, organizada por la Fundación Valenciana de Estudios Avanzados (FVEA), desde este punto de vista «el identificar a los componentes específicos de la microbiota intestinal que activan ese proceso inflamatorio es clave porque nos va a permitir identificar las dianas sobre las que tenemos que actuar para desarrollar estrategias preventivas para estas patologías».
Inmunidad innata
Ha recordado que esta relación se ha establecido sobre todo a través de estudios realizados en animales de experimentación. El ejemplo más significativo y mejor demostrado «es que las dietas ricas en grasa que conducen a la obesidad provocan una expansión de bacterias Gramnegativas, que tienen un componente en su pared celular, el lipopolisacárido (LPS), que activa la inmunidad innata y produce inflamación en el intestino. Además, este LPS pasa a circulación periférica y de ahí llega a los tejidos, influyendo e inflamando aquéllos que están implicados en el metabolismo de la glucosa, causando resistencia a insulina».
Otros estudios en animales de experimentación también indican que otros componentes bacterianos (ADN, peptidoglicano) y sus metabolitos (sulfuro de hidrógeno) pueden contribuir a la inflamación, aunque se dispone de menor información. En esta línea, otros análisis experimentales también han demostrado la posibilidad de revertir el proceso inflamatorio mediante la administración de bacterias intestinales con propiedades antiinflamatorias. Como ejemplo, Sanz ha señalado que «algunas bacterias que nosotros hemos aislado de niños lactantes sanos y que sabemos que tienen una relación negativa con el desarrollo de la obesidad, en concreto, una bifidobacteria (Bifidobacterium pseudocatenulatum CECT 7765) y un bacteroide (Bacteroides uniformis CECT 7771), revierten este proceso y reducen la inflamación a nivel intestinal y periférico y mejoran la tolerancia a la glucosa y la sensibilidad a la insulina». Los estudios preclínicos apuntan a que la inflamación va a ser una de las dianas fundamentales y permitirá «establecer estrategias de intervención dietéticas que sean preventivas, que es el papel fundamental de la alimentación».
Primeras pruebas
Sanz también ha matizado que «estos aspectos deben corroborarse con ensayos en humanos», resaltando que, «de hecho, las relaciones entre microbiota e inflamación asociada a la obesidad a este nivel aún no están bien establecidas». A pesar de estar en fases iniciales en nuestra especie, el equipo realiza un estudio en adolescentes con obesidad que tienen además resistencia a insulina y, por tanto, alteraciones en parámetros de inflamación.
«El futuro y los estudios a más largo plazo nos van a permitir reproducir a nivel de laboratorio el ecosistema intestinal de forma más aproximada y producir a gran escala otras bacterias intestinales que hasta ahora no se han utilizado en alimentación ni en medicina y que seguramente van a ser más efectivas aún», según Yolanda Sanz, del Consejo Superior de Investigaciones Científicas en el Instituto de Agroquímica y Tecnología de Alimentos de Valencia (IATA-CSIC). En este sentido, ha hecho hincapié en que «en el ecosistema intestinal existe una riqueza y una biodiversidad microbiana tremenda que no sabemos explotar, pero precisamente son las bacterias residentes en nuestro propio intestino las que están regulando nuestra salud».
Aplicaciones prácticas
Así, justifica que en la medida en que se identifiquen las bacterias o consorcio de bacterias que aportan beneficios, se aprenderá a cultivarlas y producirlas en laboratorio, «trasladando todos estos hallazgos en aplicaciones prácticas». Sanz ha apuntado que una vía es «utilizar consorcios de bacterias que formen un ecosistema estable y que puedan reemplazar la microbiota perjudicial de individuos con afectación de ciertas patologías o riesgo de padecerlas».
La investigadora va a coordinar un proyecto europeo del VII Programa Marco, de cinco años de duración, que integra a 30 socios internacionales «en el que se identificarán los consorcios de bacterias implicadas en el metabolismo de nutrientes, el balance energético y la obesidad y sus comorbilidades y en el comportamiento».
Fuente: Diario Médico 12/03/2014
. En: NotiGastro. ![]()
Los microorganismos de la microbiota intestinal podrían jugar un papel importante en el desarrollo de cáncer colorrectal.
Los microorganismos de la microbiota intestinal podrían jugar un papel importante en el desarrollo de cáncer colorrectal, según revela un estudio que se publica hoy en The Journal of Experimental Medicine.
Sergio Lira y su equipo de la Facultad de Medicina Icahn en Mount Sinai, Nueva York, partieron de la constatación previa de que la genética no lo explica todo en este tipo de tumores.
En el nuevo estudio, trataron a ratones con antibióticos para destruir su microbiota. Este tratamiento previno la formación de pólipos, lo que demostraría que las bacterias son esenciales para el desarrollo tumoral inicial en este modelo murino.
Los autores creen que los microorganismos podrían atravesar el intestino hacia el tejido de la pared intestinal, induciendo la inflamación que promueve el crecimiento tumoral.
Fuente: Diario Médico 04/03/2014
. En: Artículos de autores cubanos. ![]()
La revista electrónica MEDISAN incluye en su entrega más reciente los siguientes trabajos que tratan temas sobre enfermedades digestivas:
- Caracterización clinicoendoscópica e histológica de las afecciones digestivas. Autores: Suárez Borges M y cols. Fuente: Medisan. 2014; 18 (3).
- Isquemia Intestinal. Autores: Guerra Macías I, Rodríguez Fernández Z. Fuente: Medisan. 2014; 18 (3).
. En: NotiGastro. ![]()
El programa, puesto en marcha en el Hospital del Mar, genera además un ahorro en el coste por paciente de alrededor del 18%.
Hepatólogos del Hospital del Mar han desarrollado un Programa de Apoyo Multidisciplinar dirigido a pacientes con hepatitis C crónica que ha logrado aumentar en un 16% la adherencia al tratamiento. La evaluación de esta nueva estrategia de abordaje de la enfermedad se publica en Journal of Hepatology.
El Programa de Apoyo Multidisciplinar desarrollado en el Hospital del Mar fue llevado a cabo por dos hepatólogos, dos enfermeras, un farmacéutico, un psicólogo, un psiquiatra y apoyo administrativo. Las enfermeras y los hepatólogos proporcionaron información a los pacientes sobre la epidemiologia de la Hepatitis C, su evolución, diagnóstico y seguimiento, así como el tratamiento antiviral. El farmacéutico reforzó las instrucciones de los medicamentos y promovió la adherencia al tratamiento, y el psicólogo y el psiquiatra permitieron la detección termprana y el tratamiento eficaz de los trastornos psiquiátricos asociados.
«Lamentablemente, las características del tratamiento y las comorbilidades psiquiátricas son comunes en pacientes con hepatitis C y esto condiciona su adherencia al mismo, su resultado y la evolución de la enfermedad. Por ello es importante desarrollar programas específicos que eviten estos condicionantes a la efectividad del tratamiento» explica Ricard Solà, responsable del área de Hepatología del Hospital del Mar e impulsor del proyecto.
Ahorro en el coste por paciente
Según Solà, la información aportada a los pacientes acerca de la importancia del buen cumplimiento del tratamiento, así como la vigilancia estricta del equipo de apoyo multidisciplinario durante el proceso han sido los factores claves para el éxito del programa. Asimismo, añade, se ha comprobado que la utilización del Programa de Apoyo Multidisciplinar ha sido eficiente también económicamente, a nivel de coste-eficacia. Los pacientes con genotipo 1 incluidos en el programa alcanzaron la curación en el 62,5% de los casos, un 14,5% más que los tratados de forma convencional. El coste por paciente fue de 13.319 euros en el grupo multidisciplinar y de 16.184 euros en el grupo control. Además, el grupo de apoyo multidisciplinar logró un aumento significativo de los años de vida ajustados por calidad (AVAC) de 16,3 AVAC respecto a 15,8 AVAC en los controles.
«Los resultados demuestran que la aplicación de un programa de este tipo puede ayudar a individualizar el tratamiento, mejorar el manejo de los efectos secundarios así como la identificación de los factores de riesgo. Además, creemos que los buenos resultados obtenidos avalan el coste-efectividad y en definitiva, la utilidad de un Programa de Apoyo Multidisciplinar también en otras patologías con características parecidas», concluye el Dr.Solà.
Fuente: JANO.es · 13 Marzo 2014
. En: De la Sociedad Científica. ![]()
 La Junta Directiva de la Sociedad Cubana de Gastroenterología convoca a todos los interesados a participar en sesión científica a celebrarse el próximo miércoles 26 de marzo de 2014, a partir de las 09:00 horas, en el salón de conferencias del Hospital Clínico-quirúrgico «Hermanos Ameijeiras». El tema a tratar está relacionado con el cuidado y conservación de los endoscopios y será desarrollado por los especialistas del Centro Nacional de Ingeniería Clínica.
La Junta Directiva de la Sociedad Cubana de Gastroenterología convoca a todos los interesados a participar en sesión científica a celebrarse el próximo miércoles 26 de marzo de 2014, a partir de las 09:00 horas, en el salón de conferencias del Hospital Clínico-quirúrgico «Hermanos Ameijeiras». El tema a tratar está relacionado con el cuidado y conservación de los endoscopios y será desarrollado por los especialistas del Centro Nacional de Ingeniería Clínica.










Los lectores comentan