Trabajo publicado por la Dra. Yaimara Z. Hernández Puentes, del Hospital Militar Central «Dr. Carlos J. Finlay», Universidad de Ciencias Médicas de las FAR. Ampliar…
Trabajo publicado por la Dra. Yaimara Zunen Hernández Puentes del Hospital Militar Central «Dr. Carlos J. Finlay» de La Habana, y un equipo de investigadores, en la Revista Cubana de Medicina Militar. Ampliar…
Según un estudio del Instituto Maimónides de Investigación Biomédica de Córdoba (Imibic), este mineral reduce las lesiones de calcificación una vez que éstas ya se han formado, con lo que las células que habían comenzado a presentar características óseas vuelven a ser musculares.
Investigadores del Grupo Metabolismo del Calcio y Calcificación Vascular perteneciente al Imibic y al Hospital Universitario Reina Sofía de la capital cordobesa han demostrado cómo el magnesio previene y revierte determinados procesos relacionados con la rigidez de los vasos sanguíneos.
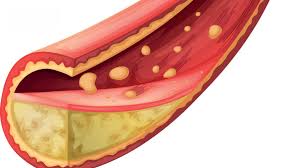
Esto procesos, conocidos como calcificación vascular, se producen cuando las células musculares de las arterias comienzan a acumular calcio y adquirir características más propias del hueso que del músculo. De esa forma, pierden la elasticidad que necesitan para contraerse y transmitir el pulso, lo que está asociado a procesos de hipertensión y otras disfunciones cardiovasculares.
Según apuntan los investigadores, se trata de una enfermedad que está asociada a alteraciones del metabolismo mineral que desarrollan enfermos renales crónicos en estado avanzado, provocándoles problemas de salud graves e incluso la muerte.
En el artículo «Magnesium Inhibits Wnt/B-Catenin Activity and Reverses the Osteogenic Transformation of Vascular Smooth Muscle Cells», publicado en la revista PlosOne (doi: 10.1371/journal.pone.0089525), los científicos han estudiado los estímulos y mecanismos que hacen aumentar y disminuir la calcificación de las células presentes en las arterias y han demostrado que un aporte adicional de magnesio disminuye y revierte esta calcificación.
«Cuando los niveles de fósforo de los pacientes renales aumentan las arterias comienzan a perder sus propiedades musculares y a transformarse en células similares a las encontradas en los huesos, los osteoblastos, incrementando la expresión de genes específicos de estas células», según explica a la «Fundación Descubre» uno de los responsables del estudio, Juan R. Muñoz-Castañeda, investigador de la Universidad de Córdoba y miembro del Imibic.
En este sentido, agrega, «partiendo de ahí decidimos investigar qué factores eran capaces de impedir ese proceso y probar si el aporte adicional de magnesio tiene un efecto beneficio sobre estas células».
Para comprobar el efecto del magnesio se han realizado experimentos «in vitro», es decir, con células aisladas. «Dosis crecientes de magnesio consiguieron descender el nivel de calcificación de las células musculares del vaso sanguíneo y, además, comprobamos que este hecho coincidía con el incremento en la expresión de genes que protegen frente a la calcificación», señala Muñoz-Castañeda.
Asimismo, estudiaron los mecanismos por los cuales se desarrolla esta patología con especial interés en el papel de la ruta imprescindible para la formación de los huesos, la llamada «Wnt/beta-catenina». «Por un lado observamos que el fósforo interviene en el proceso de calcificación activando esta ruta. Posteriormente, comprobamos que al añadir magnesio se inhibían los efectos del fósforo y de forma específica la activación de la ruta «Wnt/beta-catenina», precisa.
Además, demostraron que el magnesio era «capaz de reducir las lesiones de calcificación una vez éstas fueron formadas. Así, las células que habían comenzado a tener características óseas volvían a ser musculares y a su estado inicial, revirtiendo el proceso de calcificación», según detalla Muñoz-Castañeda.
Investigación con pacientes
Paralelamente a este proyecto, se han realizado otros estudios «in vivo», es decir, en animales que validan las conclusiones obtenidas «in vitro». Según apuntan los expertos, el siguiente paso sería comprobarlo en pacientes, ya que aún no hay ensayos controlados donde se evalúe el efecto de aumentar el magnesio en pacientes.
«No obstante, estos resultados deben ser validados in vivo dado que la compleja regulación del metabolismo mineral desencadenada durante la enfermedad renal puede verse alterada por lo que la consecuencias de estos cambios deben ser cuantificadas y evaluadas», apunta Muñoz-Castañeda.
Estos resultados se enmarcan en el proyecto de excelencia financiado por la Consejería de Innovación, Ciencia y Empresa de la Junta de Andalucía titulado «Papel de las células madre adultas y el músculo liso vascular en el daño inducido por la calcificicación vascular. Relación entre fósforo, Wnt/Beta-cateninta y osteogénesis», cuyo investigador principal es Mariano Rodríguez Portillo, catedrático del departamento de Medicina de la Universidad de Córdoba y director del grupo de investigación Metabolismo del Calcio y Calcificación Vascular del Imibic.
junio 23 /2014 (JANO)
Addy Montes de Oca, Fatima Guerrero, Julio M. Martinez-Moreno, Juan A. Madueño, Carmen Herencia, Juan R. Muñoz-Castañeda.Magnesium Inhibits Wnt/β-Catenin Activity and Reverses the Osteogenic Transformation of Vascular Smooth Muscle Cells.PLOS ONE. 25 Feb 2014
En: Noticias ![]()
En un análisis de patrones de presión arterial durante un periodo de 25 años en individuos desde jóvenes a maduros, aquéllos que presentaban niveles elevados o en aumento, durante este tiempo, tenían más posibilidades de tener unas medidas altas de calcificación arterial coronaria (CAC), según un estudio publicado en JAMA (doi:10.1001/jama.2013.285122.).
cien-hipertensionNorinna Allen, de la Facultad de Medicina Feinberg de la Universidad Northwestern (EEUU) y sus compañeros identificaron patrones comunes de la presión sanguínea durante la juventud y determinó su asociación con la presencia de CAC en la madurez entre los 4861 participantes en el estudio.
Los participantes eran blancos y negros, hombres y mujeres, desde los 18 a los 30 años al principio del estudio en 1985. Se recopilaron datos de presión arterial sistólica, diastólica y media durante los 25 años de seguimiento. El resultado primario extraído del estudio fue un alto nivel de CAC detectado por TC.
Los investigadores identificaron cinco patrones distintos en la presión arterial media: el 22 % de los participantes mantuvieron la presión sanguínea baja durante el seguimiento (grupo de baja-estable), el 42 % tenía niveles moderados (grupo de moderada-estable); el 12 % empezaron con una presión arterial moderada que incrementó en una media de 35 años (grupo de moderada-en aumento); el 19 % tenía unos niveles relativamente altos (grupo de elevada-estable) y el cinco por ciento empezaron con unos niveles elevados que aumentó durante el seguimiento (grupo de elevada- en aumento).
La prevalencia de un resultado alto de CAC variaba del cuatro por ciento en el grupo de patrón baja-estable hasta el 25 % en el grupo de patrón elevada-en aumento. Los participantes que tenían unos niveles elevados durante el periodo de estudio y a los que les aumentaban tenían mayores posibilidades de tener un nivel alto de CAC.
«A pesar de que la presión sanguínea ha sido un factor de riesgo conocido de las enfermedades cardiovasculares durante décadas, estos resultados sugieren que los patrones de cambio de un individuo a largo plazo pueden proporcionar información adicional sobre el riesgo que tiene de desarrollar una calcificación coronaria», explican los autores.
febrero 4/2014 (Diario Médico)
Norrina B. Allen, Juned Siddique, John T. Wilkins, Christina Shay, Cora E. Lewis, David C. Goff.Blood Pressure Trajectories in Early Adulthood and Subclinical Atherosclerosis in Middle Age.JAMA. 2014;311(5):490-497.
En: Noticias ![]()
Investigadores del Consejo Superior de Investigaciones Científicas (CSIC) han logrado identificar una diana potencialmente implicada en el endurecimiento de las arterias, un proceso que constituye un factor de riesgo para el desarrollo de enfermedades cardiovasculares y que constituye un fenómeno prevalente en hipertensión, aterosclerosis y durante el envejecimiento.
Según han explicado los expertos, cuya investigación ha sido publicada en la revista Molecular and Cellular Biology (doi: 10.1128/MCB.00036-13 ), la matriz extracelular, el componente orgánico existente entre las células en los organismos multicelulares, determina las propiedades de dureza y elasticidad de los tejidos, un aspecto «muy importante» en el sistema cardiovascular.
Las lisil oxidasas constituyen una familia de enzimas responsables de establecer uniones covalentes en las fibras de colágeno y elastina, en lo que supone una etapa clave en la estabilización y maduración de la matriz extracelular.
«La expresión incrementada de estas enzimas da lugar a una matriz más rígida, menos elástica, de modo que las lisil oxidasas determinan en gran medida las propiedades biomecánicas de los tejidos», ha comentado el investigador del Centro de Biología Molecular Severo Ochoa, centro mixto del CSIC y la Universidad Autónoma de Madrid, Fernando Rodríguez Pascual.
De hecho, la síntesis y deposición de componentes de matriz extracelular están reguladas por un conjunto de hormonas y factores celulares, entre los cuales el factor de crecimiento transformante (TGF-1) juega un papel relevante, directamente relacionado con el desarrollo de patologías cardiovasculares que provocan pérdida de elasticidad de los vasos sanguíneos.
En este sentido, el estudio relaciona directamente la acción del TGF-1 con un aumento notable de la expresión vascular de una forma de lisil oxidasa, la isoforma 4 (LOXL4, en inglés). «A través de este efecto sobre la expresión de LOXL4 se podría explicar la capacidad del TGF-1 de promover el endurecimiento arterial y, por consiguiente, su contribución al desarrollo de estas patologías», ha zanjado el investigador.
agosto 2/2013 (JANO)
Oscar Busnadiegoa, José González-Santamaríaa, David Lagaresb, Juan Guinea-Viniegrac, Cathy Pichol-Thievendc, Laurent Mullera. LOXL4 Is Induced by Transforming Growth Factor ß1 through Smad and JunB/Fra2 and Contributes to Vascular Matrix Remodeling.Mol. Cell. Biol.vol. 33 no. 12 2388-2401.13 Jun 2013
En: Noticias ![]()
Los marcadores circulantes pueden contribuir también al pronóstico, según una investigación que acomete el aneurisma de aorta abdominal.
La investigación y los tratamientos para abordar las enfermedades vasculares son algunos de los retos de la medicina ante el crecimiento de las enfermedades cardiovasculares en nuestros días. José Luis Marín Ventura, del Instituto de Investigación Sanitaria de la Fundación Jiménez Díaz, de Madrid, ha presentado los últimos datos de su grupo en el Instituto Maimónides de Investigación Biomédica de Córdoba.
Marcadores circulantes
El trabajo de este equipo madrileño comprende la búsqueda de biomarcadores circulantes que puedan ayudar tanto en el diagnóstico y pronóstico de enfermedades vasculares (ateroesclerosis o aneurismas de la aorta abdominal), y presentar más tratamientos al identificar nuevas dianas terapéuticas frente a este tipo de enfermedades.
Marín ha explicado que después de realizar estudios iniciales de electroforesis bidimensional y análisis por espectrometría de masas (2 DE-MS) en muestras de sobrenadantes de placas ateroescleróticas carotídeas y arterias mamarias se observó que la disminución de HSP27 en plasma de pacientes podría servir como un biomarcador diagnóstico de ateroesclerosis, de forma similar a lo que ocurre para la proteína HSP70.
«El significado biológico de la disminución extracelular de estas HSP demuestra que podría estar asociada a la proteólisis de estas proteínas en el ambiente proteolítico de la placa ateroesclerótica, mientras que su disminución intracelular se asocia a mecanismos de inestabilidad de la placa ateroesclerótica», ha señalado el investigador y ha explicado cómo se pudo advertir que después de inducir el aumento de estas proteínas mediante un tratamiento derivado de la geldanamicina (17-dmag) hubo un efecto protector en las placas, disminuyendo la lesión, el estrés oxidativo, la inflamación y el contenido en macrófagos.
Proteína antioxidante
Por otra parte y en relación con lo anterior, Marín ha precisado que en una segunda etapa del proyecto de investigación se realizaron estudios de electroforesis bidimensional con una variación de la técnica que mejora la reproducibilidad (2-dige-MS) en muestras de células polimorfonucleares (PMN) de pacientes con aneurismas de la aorta abdominal.
En este caso, los niveles de la proteína antioxidante catalasa en PMN disminuyen.
Asimismo, «el plasma de pacientes con aneurisma de la aorta abdominal, en un estudio experimental de un modelo de aneurisma de la aorta abdominal, demostró que la administración de catalasa es capaz de prevenir la formación de aneurisma de la aorta abdominal. «Los estudios de proteómica no publicados que han usado cromatografía líquida y análisis por orbitrap en sobrenadantes de trombos de aneurisma de la aorta abdominal y en los que se han identificado diversas proteínas asociadas a procesos inmunes e inflamatorios, así como de estrés oxidativo, pueden servir para pronosticar la evolución de los pacientes con aneurisma de la aorta abdominal.
Se ha referido también a la presencia de peroxirredoxina, porque esta proteína en plasma se asocia con la evolución y con una cirugía más o menos temprana.
marzo 28/2013 (Diario Médico.com)
Emplean pruebas sanguíneas para predecir nivel de enzimas que facilitan progresión de aterosclerosis
Predecir cómo la aterosclerosis, la osteoporosis o el cáncer progresarán o responderán a los medicamentos en cada paciente de manera individual es difícil. En un reciente estudio los investigadores dieron un nuevo paso hacia esa meta desarrollando una técnica capaz de predecir, a partir de una muestra de sangre, la cantidad de catepsinas –enzimas que degradan proteínas y que aceleran estas enfermedades- que una persona pueda producir.
Esta información específica del paciente puede ser útil en el desarrollo de enfoques personalizados para tratar estas enfermedades destructoras de tejidos.
«Registramos una variabilidad significativa en la cantidad de catepsinas producidas por las muestras de sangre colectadas en individuos sanos que pudieran indicar que el enfoque de un cantidad se ajusta a todos para la administración de inhibidores de catepsinas pudiera no ser la mejor estrategia para todos los pacientes con estas condiciones» dijo Manu Platt, profesor asistente en el Wallace H. Coulter Department of Biomedical Engineering at Georgia Tech and Emory University.
El estudio fue publicado en línea en octubre de 2012 en la revista Integrative Biology.
Platt y colaboradores colectaron muestras de sangre de 14 individuos sanos, extrajeron los monocitos y los estimularon con ciertas moléculas para convertirlas en macrófagos u osteoclastos. Con esto, los investigadores recrearon lo que ocurre en el organismo –los monocitos reciben estas señales a partir del tejido dañado, abandonan la sangre y se convierten en macrófagos u osteoclastos que se sabe contribuyen a los cambios tisulares que ocurren en la aterosclerosis, el cáncer y la osteoporosis.
A partir de lo anterior los investigadores desarrollaron un modelo que emplea diferentes señales de quinasas del paciente colectadas a partir de los macrófagos u osteoclastos para predecir la actividad específica en los pacientes de cuatro catepsinas: K, L, S y V.
«Las quinasas son enzimas que integran los estímulos de diferentes señales solubles, celulares y físicas para generar respuestas celulares específicas» explicó Platt. «Empleando enfoques de sistemas biológicos para relacionar señales y respuestas de diferenciación celular a través de la integración de señales a nivel de quinasas, fuimos capaces de predecir matemáticamente cantidades relativas de actividad de catepsinas y distinguir qué donantes de sangre mostraban mayor actividad de catepsinas comparados con el resto».
La previsibilidad para todas las catepsinas varió de 90 a 95 % para ambos, macrófagos y osteoclastos, a pesar de existir un rango en el nivel de cada catepsina en las muestras de sangre analizadas.
«Estamos muy satisfechos con los resultados porque nuestro modelo alcanzó un nivel de predicción muy alto desde la simple extracción de sangre y superó el reto de incorporar las señales complejas y desconocidas de los fondos genéticos y bioquímicos únicos de cada paciente», dijo Platt.
Según Platt, el siguiente paso será evaluar la capacidad del modelo para predecir la actividad catepsina usando muestras de sangre de individuos con las enfermedades de interés: aterosclerosis, osteoporosis o cáncer.
«Nuestro objetivo final es la creación de una técnica que informe al médico si el caso de una persona con cáncer u otra enfermedad destructiva del tejido va a ser muy agresivo a partir del momento en que la persona es diagnosticada, lo que permitirá al clínico elaborar y comenzar el mejor plan de tratamiento personalizado de inmediato», agregó Platt.
noviembre 19/2012 (Eurekalert)
Keon-Young Park, Weiwei A. Li and Manu O. Platt. Patient specific proteolytic activity of monocyte-derived macrophages and osteoclasts predicted with temporal kinase activation states during differentiation. Integr. Biol., 2012, DOI: 10.1039/C2IB20197F.
En: Noticias ![]()