Los expertos han sido capaces de visualizar, con detalle atómico, la estructura de un miembro de la familia de las proteínas HAT. Los resultados facilitarán el diseño de fármacos contra varias enfermedades prevalentes.
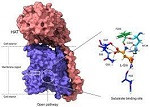 Los aminoácidos, los ladrillos básicos que permiten la vida, entran y salen de las células para que estas puedan crecer, dividirse y desarrollar sus funciones fisiológicas. Esta entrada y salida sucede gracias a las compuertas conformadas por, entre otras, las proteínas de la familia HAT, que se encuentran embebidas en la membrana celular.
Los aminoácidos, los ladrillos básicos que permiten la vida, entran y salen de las células para que estas puedan crecer, dividirse y desarrollar sus funciones fisiológicas. Esta entrada y salida sucede gracias a las compuertas conformadas por, entre otras, las proteínas de la familia HAT, que se encuentran embebidas en la membrana celular.
A pesar de que dichas proteínas son prácticamente idénticas en su estructura, unas transportan unos aminoácidos y no otros, lo que les confiere funciones completamente distintas, como aquellas relacionadas con el crecimiento de las células y su implicación en enfermedades como el cáncer, el funcionamiento de las neuronas o el transporte de sustancias tóxicas y su intervención en la adicción a sustancias como la cocaína.
“La naturaleza ha resuelto el problema de armonizar la concentración adecuada de cada aminoácido en sangre y en las células, y el flujo de aminoácidos entre células y órganos, con unos 60 transportadores distintos, que lógicamente son promiscuos y transportan varios pero no todos los aminoácidos”, explica a SINC Manuel Palacín, investigador del Instituto de Investigación Biomédica (IRB Barcelona).
Las proteínas HAT son prácticamente idénticas en su estructura. Sin embargo, unas transportan unos aminoácidos y no otros, lo que les confiere funciones distintas.
“Unos transportadores se expresan en unas células y otros en otras. Además, a tiempos distintos de nuestro desarrollo y envejecimiento. La especificidad en este escenario es necesaria, consustancial y paradigmática”, detalla a SINC el investigador, catedrático de la Universidad de Barcelona.
Tanto los científicos del IRB Barcelona como del Centro Nacional de Investigaciones Oncológicas (CNIO), se preguntaron qué es lo que confiere esta especificidad y diversidad de funciones. Por ello, analizaron la arquitectura tridimensional de esta importante familia de proteínas. Los resultados del estudio se publican en la revista Proceedings of the National Academy of Sciences (PNAS).
Vea la noticia completa en: diciembre 01/2021 (SINC)
Referencia:
Rodríguez C. F:, Escudero-Bravo P., Díaz L., Bartoccioni P., GarcíaC.: Structural basis for substrate specificity of heteromeric transporters of neutral amino acids. PNAS. 2021. DOI: 10.1073/pnas.2113573118
Tomado de: Noticias Al Día. Diciembre 2, 2021.











Haga un comentario